네이버 카페 '지성아빠의 나눔세상' 에서 제가 2021년부터 연재하던 글입니다.
여기로 복사해서 옮겨옵니다.
[ 머리말 ]
식물은 햇빛과 물,공기,흙에서 필요한 모든 양분을 얻습니다. 그렇게 진화해 왔습니다.
그럼에도 우리가 비료를 사용하는 이유는
1. 땅이 감당할 수 없을만큼 밀식 재배를 하기 때문이고
2. 유기물(곤충의 사체, 식물의 잔사와 부산물)이 땅으로 돌아갈 길을 막기 때문입니다.
넣는 것은 쉽지만 빼는 것은 아주 어렵습니다.
과한 것은 모자란 것보다 못합니다.
백 명의 농부에게는 백 가지의 다른 농사법이 필요합니다.
이 글이
무엇을 구입해서 어떻게 더 넣어줄까 하는 고민이 아닌
보다 더 균형있는 생태계와 건강한 환경을 만드는
본인만의 농사법에 대한 고민의 시작이 되기를 희망합니다.
그 시작은 자신이 키우는 식물을 잘 아는 것이겠죠.
이전 게시글을 먼저 읽고 이 글을 읽으시면 이해하는데 도움이 됩니다.
[ 영양분의 선택과 이동성 ]
이런 말 들어보셨나요?
"칼슘은 이동성이 낮기 때문에 엽면시비를 해 줘야 한다"
"토양과 강하게 흡착되어 불용화된다"
"길항 작용을 하기 때문에"
듣고 기억하고 계시다면, 관심이 아주 많은 분이시겠죠.
식물의 생리나 토양의 성질, 비료, 심지어 농약에 대해 자료를 찾아도 항상 나오는 말입니다.
나름 과학적으로 농업에 접근하고 싶은데 말처럼 쉽지는 않을겁니다.
조금 어려울수도 있는 내용인데,
머리 아픈 분들은 설렁설렁 넘기시고, 궁금증을 풀고 싶으신 분들은 두 번 세 번 읽어보시길 권해드립니다.
조금만 아는 것은 아예 모르는 것보다 위험할 수 있습니다.
1. 토양 입자는 표면에 음전하를 가지고 있습니다.
▶ 교질 ( 콜로이드, Colloid )
토양 교질(콜로이드)은 토양 중 콜로이드 성질을 나타내는 미세한 입자를 말합니다.
※ 콜로이드 성질이란
수분이나 이온을 다량 결합하며, 물 속에서는 거의 가라앉지 않고, 물이 증발하면 젤 형태로 굳어지는 성질입니다.
토양 교질은 두 종류로 구분됩니다.
1) 유기 교질 : 유기물의 분해물인 부식을 말합니다. 흔히 말하는 부엽토에 있는 주 성분입니다.
2) 무기 교질 : 암석광물이 풍화되어 토양생성과정에서 재합성된 미세한 점토광물입니다.
토양 교질은 입자가 매우 작아서 표면적이 크고, 양분과 수분을 결합하고 방출하는 역할을 합니다.
토양 교질은 음전하를 띱니다.
2. 양분은 물에 녹아서 이온 상태로 토양 용액속에 있습니다.
2.1 양이온
- 칼슘은 Ca2+ , 칼륨은 K+ , 질소(암모늄)은 NH4+ , 나트륨은 Na+ ,
- 마그네슘은 Mg2+ , 아연은 Zn2+ , 수소는 H+ , 철은 Fe2+ , 망간은 Mn2+
양이온은 이런식으로 존재합니다.
2.2 음이온
- 인은 H2PO4− , 염소는 Cl− , 황은 SO42− , 질소(질산)는 NO3−
3. 음전하에는 양전하가 붙습니다.
토양 표면이 음전하를 띠니까 음이온은 밀어내고, 양이온이 붙겠죠?
그래서
양이온은 토양과 흡착한다 라고 말하고, 음이온은 토양에 흡착되지 않고 유실 우려가 크다고 말합니다.
위의 설명을 보면 중복되는게 있죠?
질소 입니다.
▶ 양이온을 가진 질소(암모늄, NH4+)는 암모늄태 질소 라고 부르고
▶ 음이온을 가진 질소(질산, NO3−)는 질산태 질소 라고 부릅니다.
암모늄태 질소는 토양에 잘 흡착되어 유실 우려가 적고
질산태 질소는 토양에 흡착되지 않고 유실 우려가 큽니다.
질소비료에 대해서는 다음 기회에 이야기를 더 해보도록 하고,
조금만 더 나가보겠습니다.
4. 양이온 교환
음이온을 띤 토양입자에는 양이온이 붙습니다.
바깥쪽으로 갈수록 붙는 힘이 약해져서 누군가 더 잘 붙는 놈이 오면 자리를 바꿉니다.
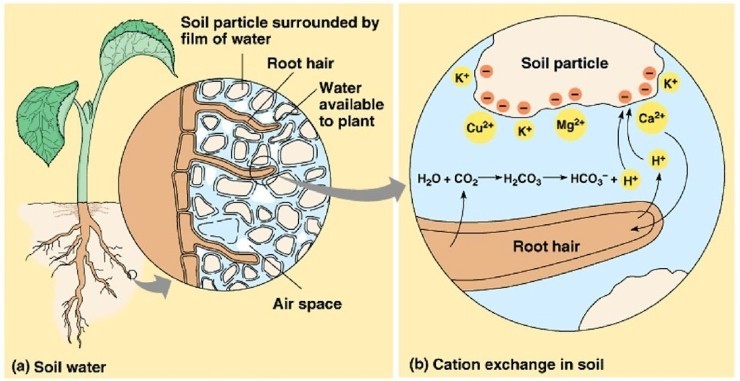
▶ 토양에 결합되어 있다가 누가 오면 자리를 내어주는 양이온을 교환성 양이온(Exchangeable cation)이라 하고,
▶ 토양에 결합할 수 있는 양이온의 크기를 양이온 교환 용량 (Cation exchange capacity, CEC) 라고 합니다.
양이온 교환 용량을 양이온 치환 용량 이라고 부르기도 합니다.
양이온 교환 용량이 클수록 토양에 있는 양분을 유실하지 않고 갖고 있다가 작물이 필요로 할 때 공급해 주므로
양이온 교환 용량 = 양분 공급 능력
이렇게 볼 수 있습니다.
+ 가 한 개 붙은 이온보다, + 가 두 개 붙은 양이온이 토양과 결합하려는 능력이 더 큽니다.
칼슘 이온이 토양 교질에 결합하려는 힘이 가장 큽니다.
이온의 농도가 높을수록, 이온의 이동 속도가 빠를수록 토양 교질에 결합하려는 힘은 커집니다.
결합하려는 힘이 약할수록, 떨어져 나오려는 힘이 커집니다.
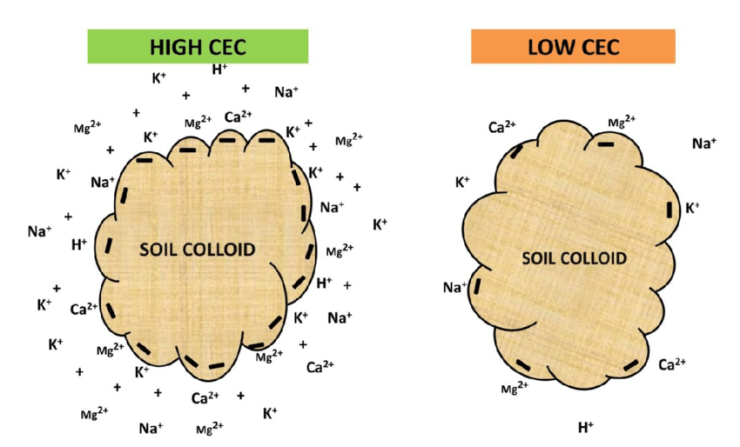
일반적으로 토양 교질 (부식, 점토)이 많을수록 양분 보유 능력 (양이온 교환 용량) 이 큰데,
유기 교질인 부식의 양분 보유 능력 (양이온 교환 용량)이 가장 큽니다.
- 양분 보유 능력 (양이온 교환 용량)이 큰 토양 = 양분이 많은 토양 = 비옥한 토양
- 양분 보유 능력 (양이온 교환 용량)이 큰 토양 = 완충 작용이 큰 토양 = 작물이 안정적으로 잘 자라는 토양
토양의 양분 보유 능력 (양이온 교환 용량)을 높이기 위해서는
1) 유기물을 넣어주거나
2) 점토가 많은 토양으로 객토하거나
3) 석회를 사용합니다.
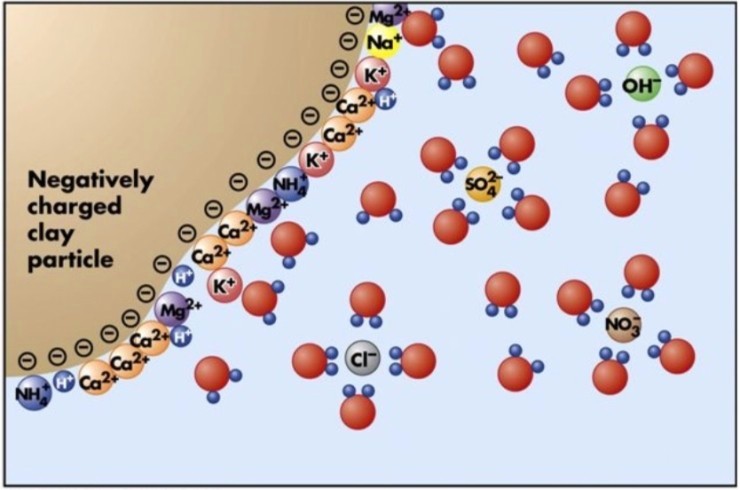
※ 토양 교질이 많으면 산성 물질이 유입되어도 토양 산도가 급격하게 변하지 않습니다.
토양 교질이 없으면 산성 물질이 유입될 경우 토양 산도가 급격하게 변하고 식물이 영향을 받습니다.
이것을 완충 작용 ( Buffer action )이라고 부릅니다.
※ 토양교질(부식이나 점토)이 거의 없는 마사토(굵은모래)만으로 이루어진 흙에 비료를 넣는 것은
밑빠진 독에 물붓기 입니다. 양분이 붙을 곳이 없습니다. 밑빠진 독이니 물빠짐은 좋겠죠?
5. 토양이 산성 토양이라면?
1) 유기 교질인 부식은 산성 조건에서 암모늄기에 의해 양전하를 나타냅니다.
2) 무기 교질도 알루미늄이나 철 등의 수산화물은 양전하를 나타냅니다.
산성 토양일때는
토양 교질이 양전하를 나타내고, 음전하와 결합합니다. 위의 설명과 반대 현상이 일어납니다.
토양 교질에 붙어있는 음이온과 토양 용액속의 음이온이 자리를 바꿀 수 있는데 이것을
음이온 교환 ( Anion exchange ) 이라고 합니다.
▶ 산성 토양이 되면 음전하를 가지고 돌아다니던 인산 이온이 철이나 알루미늄등의 무기교질에 붙어버립니다.
산성 토양이 되면 식물이 인산이온을 먹고 싶어도 못먹게 됩니다. 인산의 불용화 라고 부릅니다.
인산은 알칼리성 토양에서는 칼슘과 붙어서 불용화 되고, 산성토양에서는 철과 알루미늄 등에 붙어서 불용화 됩니다.
인산은 가축분퇴비에 아주 많습니다.
대부분의 경우 안줘서 식물이 못먹는게 아니고, 많이 있는데도 식물이 못먹습니다.
다시 식물이 먹을 수 있게 하려면?
토양의 pH 를 높여서 중성으로 만들어야 합니다. 그럼 비료값도 아끼고 농약값도 아낍니다.
6. 양이온과 음이온
식물은 특정 양분이 필요하다고 해서 그것만 골라서 먹지 않습니다. 그러면 참 좋을텐데요.
뿌리 옆에 있는 양분이 양이온인지 음이온인지, 그게 얼마나 많은지에 따라 흡수율이 달라질 뿐입니다.
식물은 양이온과 음이온을 사이좋게 같이 흡수합니다.
양이온을 잔뜩 먹은 식물은 다른 양이온 양분이 옆에 있어도 못먹습니다.
음이온 양분이 옆에 있으면 얼른 먹겠지요.
그래서
특정 원소가 많이 있으면 거기에 따라서 다른 원소를 못먹는 일이 생깁니다.
상황에 따라 특정 원소가 다른 원소의 흡수를 도와주는 일도 생깁니다.
이것을
길항작용 과 상조작용 이라고 부릅니다.
6.1 길항작용 ( Antagonism )
길항작용이란 어떤 이온이 다른 이온과 경쟁하며 그 이온의 흡수를 억제하는 작용을 말합니다.
- 칼륨 ( K ) ⇒ 칼슘 ( Ca ), 마그네슘 ( Mg )
- 칼슘 ( Ca ) ⇒ 마그네슘 ( Mg ), 칼륨 ( K )
- 마그네슘 ( Mg ) ⇒ 칼륨 ( K )
- 규산 ( Si ) ⇒ 칼슘 ( Ca )
- 암모늄 ( NH4 ) ⇒ 칼륨 ( K )
- 철 ( Fe ) ⇔ 망간 ( Mn ) 상호길항성
- 철 ( Fe ) ⇒ 암모늄 ( NH4 )
- 인산 ( P ) ⇒ 황산 ( SO4 )
- 칼슘 ( Ca ) ⇒ 아연 ( Zn )
- 염소 ( Cl ) ⇒ 붕소 ( B )
- 철 ( Fe ), 망간 ( Mn ), 암모늄 ( NH4 ), 황산 ( SO4 ) ⇒ 몰리브덴 ( Mo )
- 구리 ( Cu ) ⇒ 철 ( Fe )
6.2 상조작용 ( 상승작용, Synergism )
상조작용이란 어떤 이온이 다른 이온의 흡수를 촉진하는 작용을 말합니다.
- 칼륨 ( K ) ⇒ 망간 ( Mn ), 철 ( Fe )
- 인산 ( P ) ⇒ 몰리브덴 ( Mo )
- 질소 ( N ) ⇒ 마그네슘 ( Mg )
- 마그네슘 ( Mg ) ⇒ 인산 ( P )
- 규산 ( Si ) ⇒ 마그네슘 ( Mg )
7. 양분의 이동
뿌리에서 흡수된 양분은 물관을 타고 지상부로 올라갑니다.
물관은 잎의 기공까지 막힘 없이 연결되어 있습니다.
하지만 체관은 중간에 막이 있습니다. 마치 대나무와 같은 모양입니다.
그래서 양분의 종류와 결합형태에 따라서 이동이 제한되기도 합니다.
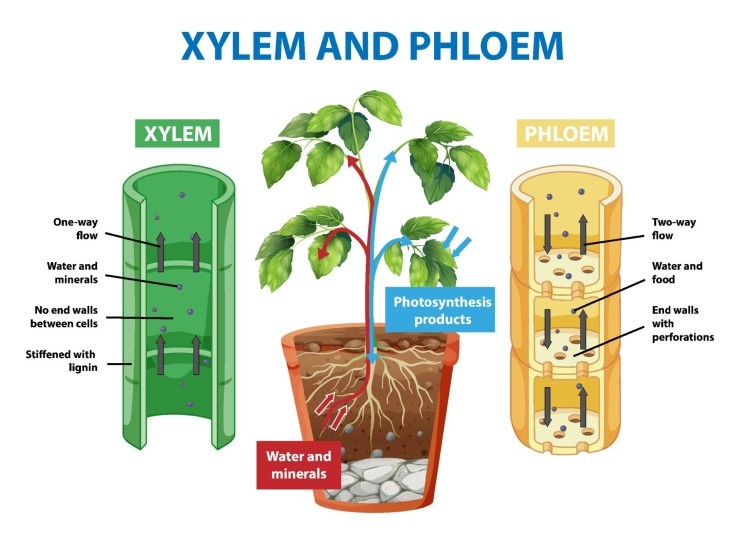
< 왼쪽이 물관이고 오른쪽이 체관입니다 >
특히 칼슘은
덩치가 커서 이 막을 잘 통과하기 힘들 뿐만아니라
이 막을 이루는 인산과 결합해서 중간에 멈추기도 합니다.
그래서 칼슘은 체관으로는 이동이 어렵고
막힘 없는 물관을 통해서만 아래쪽부터 차곡차곡 곳곳으로 공급되고 쌓입니다.
식물 내부에서 양분의 이동성은 다음과 같습니다.
- 이동이 잘 되는 양분 : 질소 ( N ), 인 ( P ), 칼륨 ( K ), 마그네슘 ( Mg )
- 이동성이 적당한 양분 : 황 ( S ), 망간 ( Mn ), 몰리브덴 ( Mo ), 아연 ( Zn ), 구리 ( Cu )
- 이동이 극히 안되는 양분 : 칼슘 ( Ca ), 철 ( Fe ), 붕소 ( B )
※ 칼슘은 미리 땅 속에 공급되어 있어야 하는 이유를 이제 아시겠죠.
칼슘이 물관을 통해서 잘 이동하려면?
잎에서 증산작용이 잘 일어나야 물의 흐름이 생기겠죠. 첫째 게시글 (식물의 영양 흡수 - 1) 을 참고하세요.
증산작용이 잘 일어나려면?
뿌리 부근이 건조하거나 과습하지 않아야 합니다.
칼슘 결핍이라고 생각될때는 더 넣을 고민보다는 다음의 내용을 먼저 확인하세요.
1) 물 주는 방법과 물빠짐 상황, 뿌리 상태 점검 (물 흡수와 증산 원활)
2) 칼륨(칼리) 비료성분을 언제 어떻게 줬는지 확인 (길항작용)
- 저작권 논란을 최대한 피해보려고 그림과 사진은 주로 외국 사이트에서 가져옵니다.
< 다음에 계속됩니다 >
'농학(農學)' 카테고리의 다른 글
| 텃밭 해충 관리 - 1 (생태계) (0) | 2024.03.26 |
|---|---|
| 식물의 영양 흡수 - 5 (호흡과 저장) (0) | 2024.03.25 |
| 식물의 영양 흡수 - 4 (광합성) (0) | 2024.03.25 |
| 식물의 영양 흡수 - 2 (필수 원소) (0) | 2024.03.25 |
| 식물의 영양 흡수 - 1 (흡수와 이동) (2) | 2024.03.25 |



